La relocalisation de la production de médicaments en cinq questions
Avec la crise sanitaire du coronavirus, l'Etat français a exprimé sa détermination à vouloir rapatrier la production de médicaments en France. Comment fabrique-t-on un médicament ? De qui la France est-elle dépendante dans la production pharmaceutique ? L'Etat mise-t-il sur les bonnes molécules ? CQFD fait le point.

Par Hélène Gully, Enrique Moreira
Assurer la souveraineté sanitaire de la France. C'est l'un des leitmotivs du gouvernement depuis la crise sanitaire du Covid-19. Afin d'éviter d'éventuelles pénuries de médicaments, le président de la République a même annoncé une enveloppe de 200 millions d'euros pour financer des infrastructures de production.
Le premier objectif que s'est fixé l'Etat : contrôler sur le territoire national l'ensemble de la chaîne de production du paracétamol, un principe actif intervenant dans plus d'une trentaine de médicaments. Avec 271 sites de production employant pas moins de 45.000 personnes sur les 100.000 qu'emploie l'industrie pharmaceutique française, la fabrication de ce médicament n'est pourtant pas en reste en France.
Alors pourquoi le gouvernement tient-il tant à rapatrier cette activité en France ? Qui sont les partenaires de l'Hexagone dans la production pharmaceutique ? L'Etat mise-t-il sur les bonnes molécules ? CQFD fait le point.
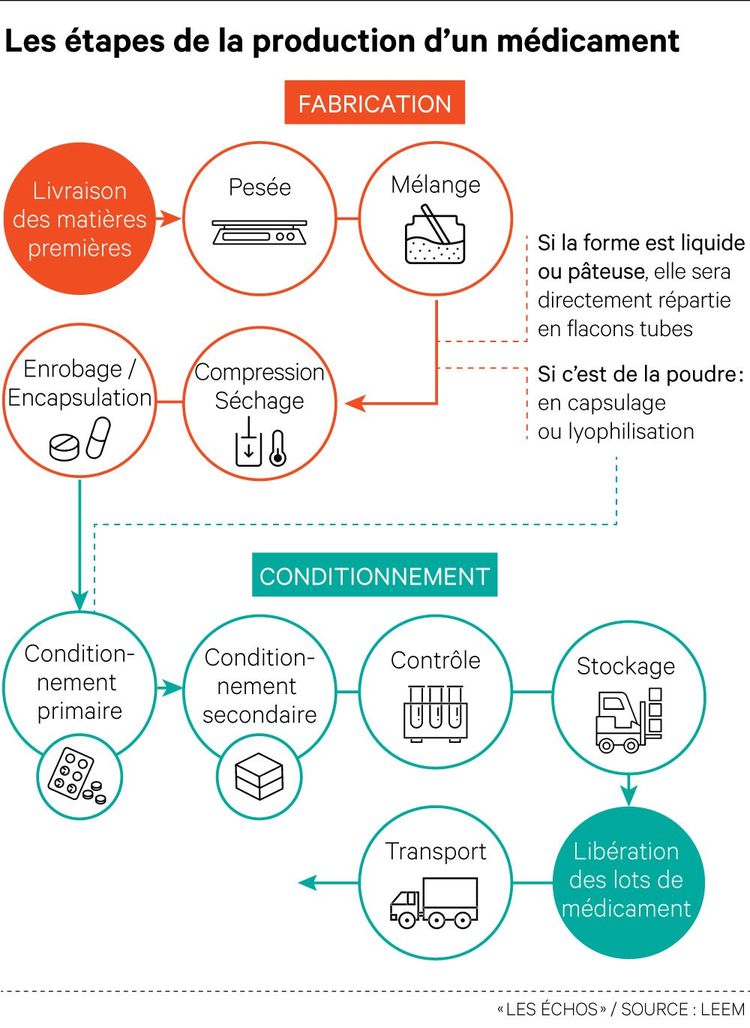
1. Comment fabrique-t-on un médicament ?
Pour comprendre les enjeux d'une potentielle relocalisation de la production pharmaceutique, il faut d'abord en distinguer les étapes. Un médicament est composé d'un ou de plusieurs principes actifs - c'est-à-dire une substance à l'origine des effets thérapeutiques - associés à des excipients. Ce médicament peut être de nature chimique ou biologique.
Il y a donc, d'une part, la production de la matière première, « la partie la plus importante », commente Marie Coris, chercheuse au GREThA, laboratoire de l'Université de Bordeaux, relié au CNRS. Et d'autre part, l'élaboration du médicament en lui-même. Ces étapes sont rarement effectuées sur un même territoire. Autrement dit : la chaîne de production d'un médicament est fragmentée entre les continents.
Les Echos
« Lorsqu'on dit que c'est produit en France par exemple, cela signifie qu'au moins une des étapes a été réalisée dans le pays, mais du 100 % made in France, c'est très très rare », recadre Marie Coris. A l'exception, probable, du paracétamol dont le gouvernement a annoncé la relocalisation totale d'ici 3 ans.
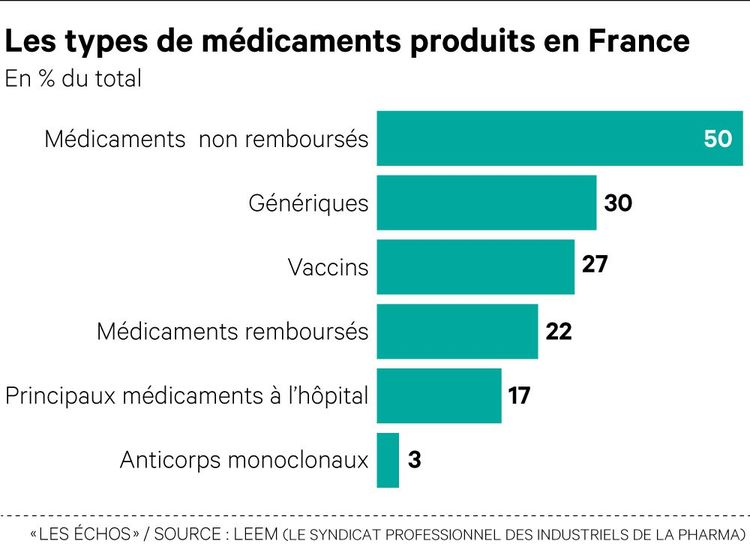
2. Quelles sont les sortes de médicaments produits en France ?
« Sur les 271 sites industriels pharmaceutiques que compte la France, 70 % fabriquent principalement trois formes galéniques (l'aspect d'un médicament, NDLR, qu'il soit composé d'une ou plusieurs molécules) : produits injectables, comprimés et spray », explique Patrick Biecheler, responsable Pharmacie monde au cabinet de conseils Roland Berger.
Sur certaines de ces formes, la France est en surcapacité de production par rapport au marché comme le montre le dernier panorama établi par le Leem, le syndicat des entreprises du médicament. C'est le cas notamment des suppositoires, des gélules et autres comprimés standards ou enrobés. Il s'agit principalement de formes dites « sèches ». A l'opposé, la production française est en sous-capacité sur des produits de types flacons stériles, hormones, les seringues préremplies ou encore les sticks pack liquides et les formes lyophilisées. Enfin, l'industrie pharmaceutique est en phase avec le marché sur des produits comme les poudres en sachet, les ampoules, les flacons ou encore les sprays.
Malgré ce tissu industriel conséquent, la France est passée en 10 ans de premier fabricant d'Europe, à quatrième, en termes de valeur de production. La faute à une activité vieillissante. « Les deux tiers des molécules qui composent ces médicaments ont en moyenne vingt ans d'existence depuis la date de publication de leur autorisation de mise sur le marché (AMM) », note Patrick Biecheler.
Cela se traduit notamment dans les aires thérapeutiques couvertes. « La production française est très présente dans les antihypertenseurs en cardiologie, les dérivés des opioïdes (douleur), les antidépresseurs ou encore le cholestérol… Ce sont les blockbusters d'avant mais aujourd'hui leurs prix sont bas », constate l'analyste. A contrario, la France produit peu dans des domaines comme les maladies auto-immunes et dégénératives, la DMLA ou encore les anticorps monoclonaux.
L'industrie pharmaceutique ne compte ainsi que 32 sites de bioproduction, fabricant des médicaments biologiques, principale des vaccins ou des protéines recombinantes. Les thérapies géniques ou cellulaires, la production de microbiote ou de tissus biologiques restent encore sous-représentées. « La France manque de structure de bioproduction capable d'accompagner la production de certains segments depuis les phases de développement jusqu'à la commercialisation », précise le panorama du Leem.
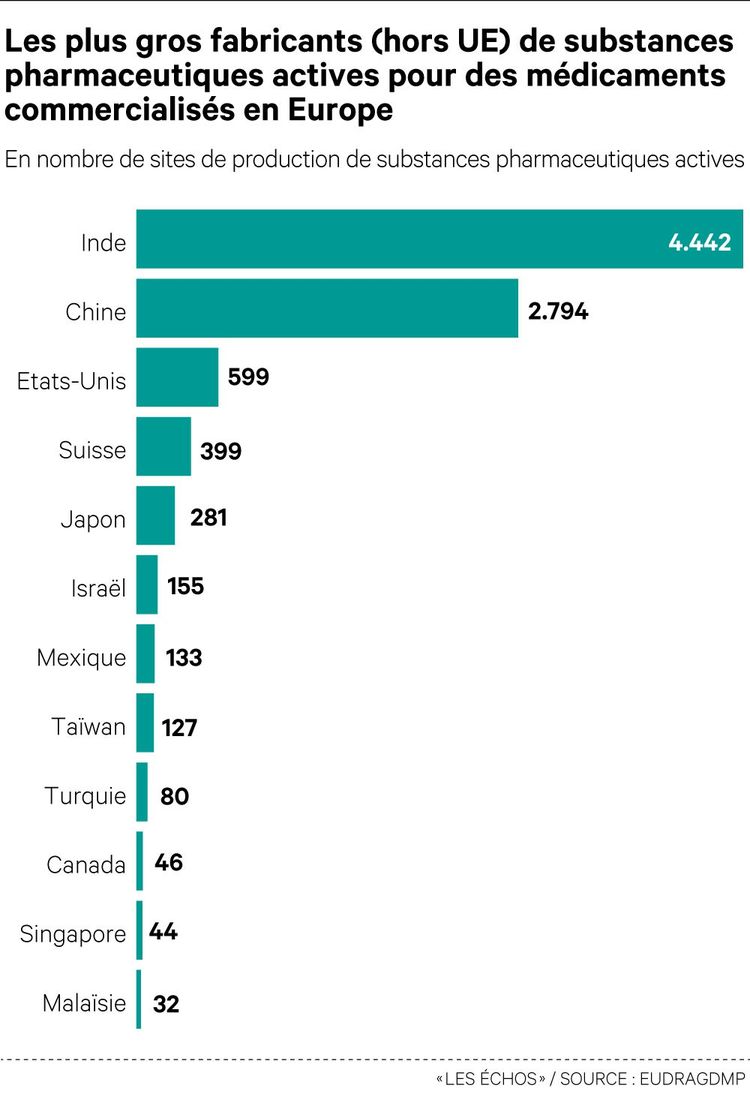
3. De qui la France est-elle dépendante et pourquoi ?
Les matières premières sont en majorité importées. Selon l'Agence européenne du médicament, 80 % des principes actifs (des médicaments disponibles dans l'UE) sont ainsi produits hors de l'Europe. Contre 20 % il y a 30 ans. En France, la situation est moins disproportionnée : « 35 % des matières premières utilisées dans la fabrication des médicaments en France proviennent de trois pays : l'Inde, la Chine et les Etats-Unis », indique un rapport du Pôle interministériel de prospective et d'anticipation des mutations économiques de 2017.
Concernant la fabrication du médicament en lui-même, environ 40 % des médicaments-finis commercialisés dans l'Union européenne proviennent de l'extérieur de l'UE, principalement d'Inde. Car la Chine et l'Inde se sont petit à petit spécialisées, la première dans la production de principes actifs, la seconde dans la mise en forme pharmaceutique et le conditionnement.
« Cette dépendance envers l'Asie n'est pas propre à la pharmacie, c'est le résultat de 40 ans de mondialisation », interprète Marie Coris. Les labos sont progressivement allés là où le coût de production était le moins cher. Notamment parce que les gouvernements (français par exemple) ont misé sur une politique de prix bas sur les médicaments. « Les firmes ont délocalisé pour tenir leurs marges, d'autant que la pharmacie est un secteur très financiarisé et que les investisseurs sont prêts à financer l'innovation à condition qu'ils bénéficient d'une rentabilité à très court terme », explique l'économiste.
L'intérêt de la délocalisation, pour les labos, s'est situé aussi dans la taille des marchés émergents. « Produire en Inde ou en Chine c'est avoir accès à des centaines de millions de consommateurs », résume Marie Coris. Enfin, les exécutifs français étaient ravis de voir certaines industries polluantes comme celle de la chimie partir ailleurs. « On a été très content d'aller polluer loin de chez nous ».
4. Quels sont les principaux freins à la relocalisation ?
L'un des principaux facteurs de fuite des industries pharmaceutiques est sans conteste le coût de production. Pour les voir revenir, il faudrait donc pouvoir combler l'écart, en augmentant par exemple le prix de vente du médicament ou en adoptant des mesures fiscales avantageuses.
Un autre paramètre particulièrement effrayant pour les industries est la réglementation. Les entreprises sont soumises à des contrôles et des normes extrêmement sévères, notamment en termes d'environnement. « Ce qui est un peu paradoxal c'est que les normes environnementales en vigueur en France sont drastiques mais que lorsqu'il s'agit d'importer, on est déjà beaucoup moins regardant », détaille Marie Coris.
Ces règles d'importation sont ainsi fortement dissuasives pour les entreprises françaises ou européennes qui ne subissent pas les mêmes exigences que leurs concurrentes étrangères, et qui sont surtout loin d'être privilégiées par leurs gouvernements. « On pourrait s'inspirer de certaines stratégies de pays émergents comme la Chine ou l'Inde qui conditionnent l'accès au marché national à des entreprises qui produisent en partie sur place », illustre l'économiste.
Selon elle, il faudrait repenser le système en profondeur et déjà travailler à une véritable politique industrielle européenne où les pays membres ne seraient pas concurrents entre eux. « Ca n'a pas de sens que de vouloir produire en France tous les médicaments majeurs dont elle a besoin, ne serait-ce que parce que le marché est trop petit », précise Marie Coris. En revanche, à défaut de tout rapatrier dans l'Hexagone, les exécutifs européens pourraient songer à une répartition entre pays membres d'une partie de la chaîne de production.
« Quand l'Europe a laissé partir la production, elle a laissé partir des compétences, la preuve avec cette crise sanitaire où l'on a vécu une dépendance à des produits de premières nécessités », rembobine l'économiste.
5. Quelles molécules choisir ?
Pour Frédéric Collet, le président du Leem, la question n'est pas tant de savoir s'il faut produire en France mais plutôt : « que veut-on y produire ? » Avec la crise sanitaire, écrivait-il dans une tribune publiée dans l'Opinion, « l'Europe a mesuré sa dépendance à l'égard de l'Asie pour la fourniture de principes actifs et de médicaments matures, comme elle pourrait l'être aussi des Etats Unis pour l'accès à certains médicaments innovants. »
L'Inde et la Chine sont en quelque sorte les champions des produits simples à fabriquer. « Il s'agit de molécules de chimie basiques que l'on peut stocker facilement car elles ont une date de péremption relativement longue », explique Patrick Biecheler. Reste à savoir si « on veut construire une usine ou un entrepôt » en France, s'interroge-t-il.
L'argent non investi dans la relocalisation pourrait alors servir à attirer des investisseurs pour développer des produits innovants, notamment de la bioproduction. Sur les 254 nouveaux médicaments autorisés par l'Agence du médicament entre 2016 et 2018, seulement 20 sont fabriqués en France. Contre 46 en Grande-Bretagne, 36 en Allemagne et 31 en Irlande.
« La construction d'une usine de biotech coûte entre 1 et 1,5 milliard d'euros. En France, seul Sanofi pourrait faire un tel investissement seul », estime Hichem Jouaber directeur associé chez AlixPartners et spécialiste de l'industrie pharmaceutique. Pour attirer ces nouveaux investisseurs, le pays devra se rendre attractif : que ce soit au niveau réglementaire (délais de recrutement des patients, d'obtention des autorisations de mise sur le marché…) mais aussi sur le plan fiscal.
Hélène Gully et Enrique Moreira

Nouveau : découvrez nos offres Premium !
Nos Vidéos

SNCF : la concurrence peut-elle faire baisser les prix des billets de train ?

Crise de l’immobilier, climat : la maison individuelle a-t-elle encore un avenir ?