Au Brésil, l’épidémie de Covid-19 est aujourd’hui dominée par plusieurs lignées virales SARS-CoV-2 qui ont toutes en commun de posséder la mutation E484K dans la protéine S (spike ou spicule), qui permet au virus de se fixer sur les cellules qu’il infecte. Cette mutation est problématique dans la mesure où elle peut contribuer à un échappement aux anticorps.
Parmi ces lignées virales brésiliennes, le variant P.1 est considéré comme préoccupant (Variant Of Concern ou VOC en anglais). Deux autres lignées, baptisées P.2 et N.9, sont considérées comme des variants à suivre, encore appelés variants d’intérêt (Variants Of Interest ou VOI en anglais).
Les variants VOC P.1 et P.2 ont évolué au Brésil à partir du même lignage (B.1.1.28) alors que le VOI N.9 dérive, lui, d’un autre lignage (B.1.1.33). Ce dernier est probablement apparu dans ce pays en août 2020 et s’est répandu dans différents états des régions Sud-Est, Sud, Nord et Nord-Est.
Le variant P.1 a été pour la première fois identifié au Japon chez des voyageurs en provenance d’Amazonas, état du nord du Brésil. Il s’est rapidement diffusé à travers tout le Brésil depuis son identification le 11 janvier 2021. Il a ensuite été établi qu’il était déjà présent dans des échantillons biologiques collectés début décembre 2020. Des analyses phylogénétiques ont montré qu’il avait probablement émergé au début ou à la fin de novembre 2020. À Manaus, capitale de l’état de l’Amazonas, la fréquence du variant P.1 a très rapidement atteint les 73 % en janvier 2021.
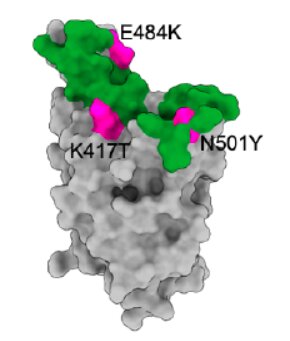
Contrairement à la lignée dont il dérive, le variant P.1 renferme les mutations E484K et N501Y, également présentes dans le variant B.1.351 identifié en Afrique du Sud. Il comporte environ 35 mutations. L’une d’elles est la mutation K417N/T, située, comme E484K, dans une région cruciale dénommée RBD, qui est le domaine de liaison de la protéine spike au récepteur cellulaire ACE2.
Le variant P.1 renferme donc trois mutations préoccupantes dans le RBD de la protéine spike : K417N/T, E484K et N501Y.
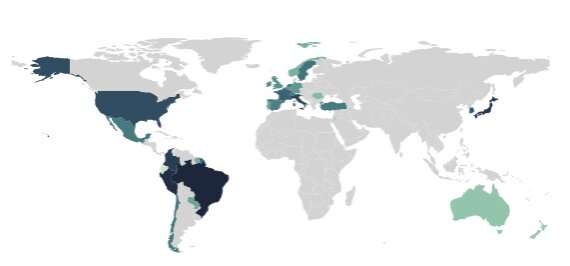
Isolé dans trente-six pays
À ce jour, outre le Brésil et le Japon, le variant P.1 a été isolé dans 34 autres pays (par ordre décroissant du nombre de séquences génétiques rapportées) : Italie, États-Unis, Belgique, Pays-Bas, Allemagne, France, Royaume-Uni, Espagne, Suisse, Portugal, Irlande, Japon, Suède, Turquie, Mexique, Australie, Nouvelle-Zélande, Jordanie, Luxembourg, Norvège, Roumanie, Singapour, Costa Rica, Aruba (Antilles néerlandaises), Iles Féroé, Corée du Sud, Slovénie, Saint-Martin (Caraïbes). En Amérique du Sud, il a été isolé au Chili, au Pérou, en Colombie, au Paraguay, en Équateur, en Guyane française et au Suriname. La semaine du 6 avril 2021, en Guyane, le variant brésilien représentait 76 % des prélèvements criblés et/ou séquencés (le variant anglais était, lui, présent à hauteur de 11 %).
En France, des enquêtes « flash », faisant appel au séquençage du génome viral sur une sélection aléatoire de prélèvements RT-PCR positifs, sont régulièrement menées. Celle du 16 mars 2021 a montré une prévalence nationale du variant P.1 de 0,5 %.
Au niveau national, Santé publique France déclarait pour la semaine du 22 au 28 mars 2021 une suspicion cumulée de variant sud-africain ou brésilien de 4,4 % sur la base de résultats de tests PCR positifs de criblage.
Chez les 10-19 ans, la proportion de suspicions de variant sud-africain ou brésilien était de 3,8 %, de 4,5 % chez les 20-29 ans, de 3,9 % chez les 40-49 ans, de 4,3 % chez les 30-39 ans, de 3,9 % chez les 40-49 ans, de 4,1 % chez les 50-59 ans. Elle est de 4,4% chez les 60-69 ans et 70-79 ans et de 4,8 % chez les 80-89 ans. Chez les personnes âgées de 90 ans et plus, cette proportion est de 5,1 %.
Un variant plus contagieux
À ce jour, les études ont estimé que le variant P.1 est 1,4 à 2,2 fois plus contagieux que la souche de référence. Publiée le 23 mars 2021 sur le site medRxiv, une étude, réalisée par des épidémiologistes de l’université fédérale de Santo André (état de São Paulo), rapporte une transmissibilité de P.1 2,6 fois plus importante par rapport à la souche de référence [1].
Au Brésil, le variant P.1 serait donc un peu plus contagieux que le variant anglais B.1.1.7 qui, lui, présente une transmissibilité accrue d’un facteur 2,3 par rapport à la souche historique de référence.
Réinfections par le variant P.1
Les estimations de cette équipe brésilienne confirment par ailleurs la capacité du variant P.1 à entraîner des réinfections, à savoir provoquer une nouvelle infection chez des individus ayant déjà été infectés par la souche ancestrale.
Selon les estimations des épidémiologistes brésiliens, les réinfections par P.1 représentaient 28 % de cas survenus à Manaus entre novembre 2020 et janvier 2021 [2].
Quid de la dangerosité du variant P.1 ?
Mais le variant P.1 est-il pour autant plus virulent que les lignées qui circulaient auparavant au Brésil ? À ce jour, les données cliniques manquent. On ignore si P.1 est associé à une charge virale plus élevée ou à une durée d’infection plus longue. En d’autres termes, la pathogénicité de P.1 est encore inconnue.
La presse brésilienne fait néanmoins état d’une augmentation de la mortalité chez des patients plus jeunes qu’auparavant. On peut cependant noter que l’on observait déjà, au début de la pandémie, plus de décès chez les patients de moins de 60 ans au Brésil par rapport à ce que l’on avait observé en Chine ou en Italie.
Afin d’en savoir plus, des épidémiologistes américains (Cincinnati, Ohio) et brésiliens (université fédérale de l’état du Parana, Curitiba) ont analysé les données sanitaires de cet état situé dans le sud du Brésil, frontalier avec l’Argentine au sud-ouest et le Paraguay à l’ouest. Publiée le 26 mars sur le site medRxiv, leur étude porte sur des informations collectées entre le 1er septembre 2020 et le 17 mars 2021. Dans l’état du Parana, le variant P.1 a été identifié pour la première fois le 16 février 2021. Depuis mars 2021, il a été isolé dans environ 70 % des échantillons biologiques collectés.
Les résultats préliminaires obtenus par Maria Helena Santos de Oliveira et ses collègues montrent que depuis la diffusion du variant P.1 on observe une augmentation du taux de létalité au Parana dans toutes les tranches d’âge, en particulier parmi les jeunes adultes et ceux d’âge moyen. Il n’a cependant pas été noté de risque accru de décès chez les enfants et les adolescents.
Plus précisément, le taux de létalité parmi les 20-29 ans a ainsi triplé entre janvier et février 2021, passant de 0,04 % à 0,13 % dans cette fourchette d’âge. Durant cette même période, il a doublé parmi les 40-49 ans, atteignant 0,9 % dans cette classe d’âge. De même, ce taux a quasiment doublé chez les 30-39 ans et les 50-59 ans. Une augmentation des décès a également été observée parmi les plus de 60 ans, mais pas dans les mêmes proportions.
Les raisons de l’augmentation du taux de létalité dans ces différents groupes d’âge ne sont pas claires. Cela tient-il à une plus forte exposition au virus parmi les adultes les plus jeunes ou à une virulence accrue du variant P.1 ? Il n’est pas possible aujourd’hui de conclure entre ces deux hypothèses. En effet, il semble difficile de distinguer entre ce qui tiendrait d’une augmentation de la virulence du SARS-CoV-2 et ce qui ne serait que la conséquence d’une pression extrêmement forte sur les hôpitaux, d’un manque de lits de soins critiques, d’un manque d’approvisionnement en oxygène, voire d’un effondrement local ou régional d’un fragile système de santé. Avec pour résultat une prise en charge médicale non satisfaisante et une mortalité plus importante.
Bien que l’on puisse penser que la transmissibilité accrue du nouveau variant P.1 a entraîné une saturation du système hospitalier et un dépassement des capacités de soins, force est de constater que l’augmentation de la létalité a pourtant coïncidé avec une baisse du nombre total de cas d’infections dans l’état du Parana, font remarquer les chercheurs. Il est donc possible que les adultes jeunes, gagnés par la « fatigue pandémique », soient moins respectueux des gestes barrières et s’exposent donc plus au virus. Cette hypothèse est cependant loin d’être pleinement satisfaisante pour expliquer la soudaine augmentation de la létalité alors même que le nombre de cas diminue.
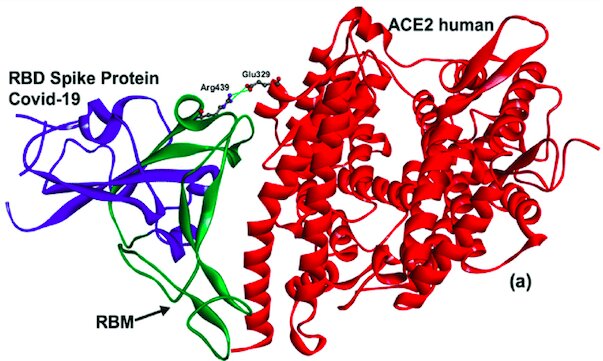
Nouveau variant N.10
Un nouveau variant, désigné temporairement N.10, a été rapporté le 7 avril 2021 par des chercheurs de l’Institut Oswaldo Cruz (Fiocruz, à Rio de Janeiro) sur le site virological.org. Ce virus renferme quatorze mutations qui font de lui, théoriquement, un nouveau VOI.
Le variant N.10 contient notamment les mutations V445A et E484K dans le RBD, le domaine de fixation de la protéine spike du SARS-CoV-2 sur le récepteur cellulaire ACE2. La mutation V445A se situe, elle, dans une boucle située dans le motif RBM (receptor binding motif). Celui-ci se trouve dans le RBD, région qui est directement en contact avec le récepteur ACE2.
Le RBM est la cible de nombreux anticorps neutralisants. Toute mutation de cette région cruciale est donc susceptible de conférer une résistance partielle du virus vis-à-vis des anticorps produits en réaction à l’infection virale.
Dans ce variant N.10, les délétions (pertes de matériel génétique) sont, elles, situées dans le NTD (domaine amino-terminal de la protéine spike), au sein ou à proximité immédiate d’un site également reconnu par les anticorps neutralisants. Ces délétions pourraient donc conférer une résistance à la neutralisation par des anticorps normalement dirigés contre le domaine NTD. Selon les chercheurs brésiliens, N.10, qui circule actuellement dans les états du nord-est du Brésil, pourrait avoir la capacité d’échapper à la fois aux anticorps anti-RBD et anti-NTD. Ils estiment donc que ce nouveau variant devrait faire l’objet d’une étroite surveillance épidémiologique.
Ce variant d’intérêt N.10 a probablement émergé fin décembre 2020, estiment Paola Cristina Resende et ses collègues du réseau de surveillance génomique Covid-19 Fiocruz qui ont séquencé des échantillons biologiques provenant du Maranhão, état du nord-est du Brésil. Ce nouveau VOI représentait 23 % des infections par le SARS-CoV-2 dans cet état entre janvier et février 2021.

Nombreux variants circulants au Brésil
Outre les variants brésiliens P.1, P.2, N.9 et N.10, le B.1.351, plus connu sous le nom de variant sud-africain, circule aussi dans tout le Brésil.
Publiée le 8 avril sur le site virological.org, une étude apporte des informations sur la fréquence des variants SARS-CoV-2 dans la région métropolitaine de Belo Horizonte, capitale de l’état de Minas Gerais, un des états les plus peuplés du Brésil avec plus de 21 millions d’habitants.
Cette enquête d’épidémiologie moléculaire a consisté dans le séquençage génomique de souches virales isolées dans 75 échantillons cliniques recueillis entre le 28 octobre 2020 et le 15 mars 2021. Pour la première fois, le variant anglais B.1.1.7 a été détecté par séquençage direct et non plus indirectement sur la négativation de la détection du gène S (S gene target failure) au test PCR. Ce résultat montre donc que le variant anglais B.1.1.7 circule aussi au Brésil.
Dans l’état de Minas Gerais, le variant anglais représente 3,5 % des souches analysées, tandis que les fréquences des variants P.1 et P.2 se situent respectivement à 35 % et 48 %. Cette co-circulation de variants dotés d’une transmissibilité accrue et d’un échappement immunitaire est contemporaine d’une récente augmentation des cas d’infections et des décès dans la région métropolitaine de Belo Horizonte.
Malgré le faible nombre d’échantillons analysés, cette étude a également montré un changement dans la composition génétique des virus SARS-CoV-2 dans la région métropolitaine de Belo Horizonte.
Alors que le variant P.2 avait été la lignée principale pendant la majeure partie de la période observée, la fréquence du variant P.1 a rapidement augmenté au cours de l’étude jusqu’à devenir la lignée dominante au cours des semaines suivantes. Au total, les trois variants P.1, P.2 et B.1.1.7 ont pris le dessus sur les lignées virales (B.1.1.28 et B.1.1.33) qui circulaient depuis le début de la pandémie dans ce vaste état du sud-est du Brésil. Ce profil de remplacement correspond à celui observé dans d’autres régions du pays, confirmant l’avantage des variants préoccupants (VOC) sur les autres lignées virales.
Cette étude, publiée le 8 avril 2021 sur le site medRxiv et coordonnée par des chercheurs des universités fédérales de Rio de Janeiro et Belo Horizonte, révèle également la circulation d’un possible nouveau variant dérivé du lignage historique B.1.1.28. Le séquençage a montré que celui-ci renferme une combinaison unique de dix-huit mutations (dont quatre dans la protéine spike). Ce variant renferme notamment de nouvelles mutations aux positions 484 (E484Q) et 501 (N501T) associées à un échappement immunitaire et une plus grande transmissibilité du virus.
Le SARS-CoV-2 continue à évoluer
Cette même équipe a rapporté que certains variants SARS-CoV-2 préoccupants et d’intérêt identifiés au Brésil ont récemment évolué de façon à présenter un jeu de pertes et de gains de matériel génétique (des insertions-délétions dénommées indels) dans le domaine NTD de la protéine spike.
Ces résultats montrent donc que le SARS-CoV-2 n’en finit pas de s’adapter et d’évoluer pour échapper aux anticorps dirigés contre la région NTD et peut-être un jour devenir encore plus résistant que les variants brésiliens actuels P.1 et P.2.
La survenue au Brésil de mutations du SARS-CoV-2 à des positions identiques à celles déjà observées ailleurs dans le monde montre qu’il existe une évolution convergente tendant à rendre le virus plus contagieux (via l’émergence de mutations dans le RBD de la protéine S). Une hypothèse est que cette évolution du génome viral se produit sous l’effet d’une intense pression de sélection au sein d’une population de plus en plus largement immunisée par l’infection naturelle.
Les chercheurs brésiliens font remarquer que leurs échantillons biologiques ont été collectés auprès d’individus non apparentés dans différentes régions de l’état de Minas Gerais, ce qui tend à montrer que ce nouveau variant d’intérêt y circule largement. Seules deux séquences de ce nouveau virus sont aujourd’hui rapportées, alors qu’il faut au moins cinq séquences porteuses d’une même signature génétique pour officiellement parler de nouveau variant. Des études sont actuellement en cours dans cette même région sur un plus grand nombre de prélèvements biologiques.
Selon Filipe Romero Rebello Moreira et ses collègues, la présence dans ce variant d’une constellation de nouvelles mutations de même que les données de l’analyse phylogénétique montrent que ce virus correspond sans doute à un nouveau VOI qui devrait être désigné P.4.
E484K, mutation d’échappement immunitaire
Ces différents variants brésiliens ont la particularité de partager la mutation E484K sur la protéine spike. Une étude américaine, publiée le 7 avril 2021 dans la revue The Lancet Microbe, confirme que E484K s’accompagne d’une diminution du pouvoir neutralisant des anticorps.
Sonia Jangra et ses collègues de l’Icahn School of Medicine du Mont Sinaï de New York rapportent une moindre efficacité des anticorps neutralisants vis-à-vis d’un virus SARS-CoV-2 dans lequel la mutation E484K a été artificiellement introduite par rapport à la souche historique USA-WA1/2020 (isolée aux États-Unis chez un individu de retour de Wuhan).
L’impact de la présence de la mutation E484K a également été observé tant chez des individus vaccinés que chez des patients Covid-19 convalescents. Lorsque la quantité des anticorps IgG développés par un individu est peu importante (titre faible), celle-ci est diminuée d’un facteur 2,4 lorsque le virus est porteur de la mutation E484K. Lorsque le titre en anticorps IgG est modéré, on observe une diminution d’un facteur 4,2. En cas de titre en IgG élevé, celui-ci est tout de même réduit d’un facteur 2,6.
Ces données montrent donc que la seule présence de la mutation E484K (dans le domaine de liaison RDB de la protéine S au récepteur cellulaire ACE2) s’accompagne d’une diminution de la capacité des anticorps neutralisants à se fixer sur leur cible, que ceux-ci aient été produits après une infection naturelle ou induits par la vaccination.
Un titre en anticorps neutralisants faible ou modéré pourrait se traduire par une perte du pouvoir neutralisant. Il apparaît néanmoins que les patients ayant développé des titres en anticorps élevés vis-à-vis de la souche historique USA-WA1/2020 sont encore capables de neutraliser un virus SARS-CoV-2 recombinant porteur de la mutation E484K. D’où l’importance que la vaccination induise un taux d’anticorps neutralisants le plus élevé possible pour assurer une protection maximale vis-à-vis de telles souches.
Du fait du manque d’approvisionnement en vaccins, certaines autorités sanitaires ont décidé de différer la seconde injection vaccinale afin de délivrer la première dose au plus grand nombre de personnes. Selon les chercheurs new-yorkais, cette approche pourrait entraîner un moindre titre en anticorps, alors que leurs résultats montrent qu’un titre insuffisamment élevé est susceptible de se révéler problématique dans un contexte d’émergence de nouveaux variants.
Cela dit, on ignore dans quelle mesure d’autres mécanismes immunologiques pourraient tout de même conférer une protection, en l’occurrence la production d’autres types d’anticorps dit non-neutralisants et plus encore la participation de lymphocytes T impliqués dans l’immunité cellulaire.
Quid de l’efficacité des vaccins ?
Salim Abdool Karim et Tulio de Oliveira (Durban, Afrique du Sud) ont rapporté le 24 mars 2021 dans une correspondance au New England Journal of Medicine que l’activité neutralisante des personnes vaccinées avec le vaccin Pfizer-BioNTech (BNT162b2) était diminuée d’un facteur 6,7 vis-à-vis du variant P.1 et d’un facteur 4,5 avec le vaccin Moderna (mRNA-1273).
À ce jour, l’impact de cette diminution de la capacité de neutralisation en termes de protection vis-à-vis d’une maladie Covid-19 modérée ou sévère n’est pas claire. Les chercheurs sud-africains précisent que l’efficacité du vaccin AstraZeneca (AZD1222) est 3,2 fois supérieure au Brésil et au Royaume-Uni à ce qu’elle est en Afrique du Sud (70 % contre 22 %) et que le vaccin de Novavax (États-Unis) est 1,8 fois plus efficace au Royaume-Uni qu’en Afrique du Sud (89% vs. 49%) [3].
Publiée le 12 mars 2021 dans la revue Cell, une étude conduite par des chercheurs du Massachusetts General Hospital de Boston a évalué la capacité neutralisante des anticorps sériques de sujets ayant reçu une ou deux doses du vaccin Pfizer ou Moderna vis-à-vis de virus porteurs à leur surface d’une protéine spike ayant subi certaines mutations [4].
Les résultats montrent que même si la neutralisation par anticorps est largement conservée vis-à-vis de variants contenant les mutations K417N/T, E484K, N501Y présentes dans le domaine RBD, en l’occurrence le variant brésilien P.1 et sud-africain B.1.351, l’activité neutralisante est cependant significativement réduite même chez les patients complètement vaccinés.
Plus précisément, l’activité neutralisante des anticorps est significativement diminuée vis-à-vis du variant brésilien P.1, en l’occurrence d’un facteur 6,7. Lors de ces expériences, les individus qui n’avaient reçu qu’une dose de vaccin ont globalement présenté une plus faible capacité de neutralisation, voire aucune activité neutralisante détectable vis-à-vis du variant sud-africain.
De même, la neutralisation du variant P.2 est significativement diminuée, d’un facteur 5,8 chez les patients ayant reçu le vaccin Pfizer et d’un facteur 2,9 chez ceux auxquels on avait administré le vaccin Moderna [5].
Quid de l’efficacité des anticorps monoclonaux ?
Publiée dans la revue Cell le 30 mars 2021, une étude dirigée par des chercheurs de l’université d’Oxford a montré que le variant brésilien P.1 peut échapper à l’activité neutralisante de certains anticorps monoclonaux dont certains ont été développés dans un but préventif ou thérapeutique. Le principe est de fournir à l’organisme des doses importantes de ces anticorps spécifiquement dirigés contre une cible particulière du SARS-CoV-2.
Il s’avère que certains anticorps monoclonaux développés par la firme Lilly n’ont pas montré d’activité neutralisante vis-à-vis de P.1. En revanche, la neutralisation d’autres anticorps, développés par les sociétés Regeneron, Adagio et AstraZeneca, n’a pas ou peu été diminuée. Il n’en a pas été de même pour le variant sud-africain B.1.351.
Le variant P.1 s’est montré significativement moins résistant aux anticorps produits par l’infection naturelle ou la vaccination que le variant sud-africain. L’activité neutralisante des anticorps générés par le vaccin Pfizer vis-à-vis du variant P.1 a été significativement diminuée d’un facteur 2,6 par rapport à la souche Victoria (apparentée au virus historique de Wuhan et ainsi dénommée car isolée en Australie). Quant à la neutralisation des anticorps produits après administration du vaccin AstraZeneca, elle a été significativement diminuée d’un facteur 2,9.
Malgré une réduction significative de l’activité neutralisante, et ses collègues estiment que l’immunisation obtenue avec les vaccins actuels, tous dirigés contre la protéine de souches ancestrales (proches du virus de Wuhan), permettra probablement de protéger contre le variant brésilien P.1. En revanche, il s’avère que la neutralisation des anticorps contre P.1 est considérablement meilleure que celle contre le variant sud-africain (réduction d’un facteur 7,6 avec le vaccin Pfizer et d’un facteur 9 avec la vaccin AstraZeneca).
La raison de cette différence concernant la neutralisation du variant brésilien P.1 et sud-africain B.1.351 n’est pas claire. Il est possible que cela reflète la présence dans le variant sud-africain de mutations situées en dehors du domaine RBD et qui lui confèreraient une plus grande capacité à échapper à l’action des anticorps neutralisants.
Une étude allemande, publiée dans la revue Cell le 20 mars 2021 et réalisée par des chercheurs de l’université Georg-August de Göttingen, a également montré que le variant P.1 est partiellement résistant à l’anticorps monoclonal casirivimab de la société Regeneron ou totalement résistant au bamlanivimab de la firme Lilly, molécules ayant reçu une autorisation temporaire d’utilisation dans le traitement de la Covid-19. Des résultats similaires ont été obtenus avec le variant sud-africain B.1.351.
Par ailleurs, l’entrée des variants P.1 et B.1.351 [5] dans des cellules était moins efficacement inhibée par le plasma de patients Covid-19 convalescents ainsi que par les anticorps sériques développés suite à l’administration de deux doses du vaccin Pfizer.
Pour Markus Hoffman et ses collègues, ces résultats semblent indiquer que les variants P.1 et B.1.351 pourraient échapper à l’activité neutralisante des anticorps chez certains individus convalescents ou vaccinés. La limitation de la circulation de ces variants par des mesures barrières demeure donc essentielle.
Nécessité du séquençage génomique
Qu’il s’agisse du variant brésilien P.1 ou de tout autre variant préoccupant (VOC) ou d’intérêt (VOI), une chose est sûre : leur émergence au cours de ces derniers mois souligne encore plus l’importance de conduire une surveillance génomique, seul moyen de les identifier précocement.
Force est de constater que la France ne brille pas par ses capacités de séquençage génomique des souches circulantes de SARS-CoV-2. Elle est loin derrière le Royaume-Uni, les États-Unis, l’Australie, les Pays-Bas, l’Espagne, l’Inde, la Chine, la Belgique, le Danemark, le Canada, le Portugal et l’Islande, lorsqu’on considère le nombre de séquences déposées dans les bases de données génomiques.
C’est grâce à une telle surveillance qu’un grand foyer épidémique (cluster) a récemment été découvert au Canada en Colombie-Britannique par des virologues de l’hôpital Saint-Paul de Vancouver. Près de 900 infections au variant P.1 ont été détectées dans cette province, dont 200 dans la station de ski de Whistler.
Développer des vaccins de nouvelle génération
L’ensemble des données concernant l’activité neutralisante des anticorps induits par la vaccination montre donc que des variants SARS-CoV-2 sont potentiellement capables d’échapper à l’immunité naturelle, voire à celle induite par les vaccins.
Ce constat rend nécessaire le développement d’une nouvelle génération de vaccins capables d’induire une large activité neutralisante vis-à-vis des variants qui circulent actuellement mais également contre ceux qui pourraient émerger à l’avenir.
Au vu des données disponibles, il apparaît que le variant sud-africain est le plus préoccupant du fait de la réduction importante de l’activité neutralisante des anticorps, voire dans certains cas de leur incapacité totale à neutraliser ce variant. Les chercheurs de l’université d’Oxford estiment que le développement de nouveaux vaccins contre le variant sud-africain constitue aujourd’hui la priorité la plus importante.
Des résultats publiés par des chercheurs français dans la revue Nature Medicine le 26 mars 2021 vont dans ce sens. Ils confirment que le variant sud-africain est moins sensible aux anticorps neutralisants.
Des chercheurs de l’Institut Pasteur, en collaboration avec plusieurs équipes hospitalières, ont évalué la sensibilité des variants anglais et sud-africain aux anticorps après infection naturelle ou vaccination. Ils ont comparé cette sensibilité avec celle obtenue vis-à-vis de la souche qui circule majoritairement en France (porteuse de la mutation D614G).
Il s’avère que le variant anglais est neutralisé par les anticorps de façon quasiment identique à cette souche de référence, alors que le variant sud-africain est, lui, moins sensible aux anticorps neutralisants. Plus précisément, Delphine Planas, Olivier Schwartz et leurs collègues ont observé une perte d’activité neutralisante contre le variant sud-africain dans 40 % des sérums des individus exposés au virus neuf mois plus tôt. Par ailleurs, des concentrations six fois plus élevées d’anticorps sont nécessaires pour neutraliser le variant sud-africain par rapport à la souche de référence.
Concernant cette fois les personnes vaccinées, les anticorps sériques de ces individus sont presque aussi efficaces contre le variant anglais que contre la souche de référence (D614G). En revanche, leurs anticorps sont moins efficaces vis-à-vis du variant sud-africain. Ainsi, 80 % des sérums sont neutralisants pour la souche de référence D614G et le variant anglais, alors que seulement 60 % des sérums sont neutralisants pour le variant sud-africain.
Mais revenons au variant brésilien P.1. Les résultats obtenus à ce jour mettent en lumière le risque que représente une transmission incontrôlée du SARS-CoV-2 dans la population brésilienne, dans la mesure où elle pourrait entraîner l’émergence de variants potentiellement encore plus contagieux.
Marc Gozlan (Suivez-moi sur Twitter, Facebook, LinkedIn)
[1] Intervalle de confiance compris entre 2,4 et 2,8, ce qui signifie que la valeur est en réalité comprise entre ces deux valeurs.
[2] Des réinfections par le variant brésilien P.2 ont également été rapportées. P.2 renferme 12 mutations dans la protéine S dont trois dans le domaine RBD.
[3] L’efficacité du vaccin AstraZeneca est supérieure aux Etats-Unis (72 %) qu’en Afrique du Sud (57 %) où circule très largement le variant B.1.351.
[4] Ces expériences ont consisté à évaluer l’efficacité de la neutralisation à l’aide de tests utilisant des pseudovirus, autrement dit de virus artificiels se comportant comme de « faux coronavirus » car porteurs à leur surface de la protéine spike du SARS-CoV-2.
[5] Ces expériences ont été réalisées en utilisant des pseudovirus (virus de la stomatite infectieuse porteurs de la protéine S du SARS-CoV-2). Ces résultats devront donc être confirmés en utilisant d’authentiques virus SARS-CoV-2.
Pour en savoir plus :
Matic N, Lowe CF, Ritchie G. Rapid Detection of SARS-CoV-2 Variants of Concern, Including B.1.1.28/P.1, in British Columbia, Canada. Emerg Infect Dis. 2021 Jun. 27(6)
Francisco RDS Jr, Benites LF, Lamarca AP, et al. Pervasive transmission of E484K and emergence of VUI-NP13L with evidence of SARS-CoV-2 co-infection events by two different lineages in Rio Grande do Sul, Brazil. Virus Res. 2021 Apr 15;296:198345. doi: 10.1016/j.virusres.2021.198345
Moreira FRR, Bonfim DM, Geddes VEV, et al. Increasing frequency of SARS-CoV-2 lineages B.1.1.7, P.1 and P.2 and identification of a novel lineage harboring E484Q and N501T spike mutations in Minas Gerais, Southeast Brazil. Virological, April 8, 2021.
Jangra S, Ye C, Rathnasinghe R, Stadlbauer D; Personalized Virology Initiative study group, et al. SARS-CoV-2 spike E484K mutation reduces antibody neutralisation. Lancet Microbe. 2021 Apr 7. doi: 10.1016/S2666-5247(21)00068-9
Resende PR, Gräf T, Lima Neto LG et al. Identification of a new B.1.1.33 SARS-CoV-2 Variant of Interest (VOI) circulating in Brazil with mutation E484K and multiple deletions in the amino (N)-terminal domain of the Spike protein. Virological. April 7, 2021.
Resende PR, Gräf T, Paixão ACD, et al. A potential SARS-CoV-2 variant of interest (VOI) harboring mutation E484K in the Spike protein was identified within lineage B.1.1.33 circulating in Brazil. Virological. April 4, 2021.
Slavov SN, Patané JSL, Bezerra RS, et al. Genomic monitoring unveil the early detection of the SARS-CoV-2 B.1.351 lineage (20H/501Y.V2) in Brazil. medRxiv. Posted April 04, 2021. doi: 10.1101/2021.03.30.21254591
Dejnirattisai W, Zhou D, Supasa P, et al. Antibody evasion by the P.1 strain of SARS-CoV-2. Cell, Available online 30 March 2021. doi: 10.1016/j.cell.2021.03.055
Planas D, Bruel T, Grzelak L, et al. Sensitivity of infectious SARS-CoV-2 B.1.1.7 and B.1.351 variants to neutralizing antibodies. Nat Med. 2021 Mar 26. doi: 10.1038/s41591-021-01318-5
Abdool Karim SS, de Oliveira T. New SARS-CoV-2 Variants – Clinical, Public Health, and Vaccine Implications. N Engl J Med. 2021 Mar 24:NEJMc2100362. doi: 10.1056/NEJMc2100362
Hoffmann M, Arora P, Groß R, et al. SARS-CoV-2 variants B.1.351 and P.1 escape from neutralizing antibodies. Cell. 2021 Mar 20:S0092-8674(21)00367-6. doi: 10.1016/j.cell.2021.03.036
Resende PC, Naveca FG, Lins RD, et al. The ongoing evolution of variants of concern and interest of SARS-CoV-2 in Brazil revealed by convergent indels in the amino (N)-terminal domain of the Spike protein. Virological, March 18, 2021.
Garcia-Beltran WF, Lam EC, St Denis K, et al. Multiple SARS-CoV-2 variants escape neutralization by vaccine-induced humoral immunity. Cell. 2021 Mar 12:S0092-8674(21)00298-1. doi: 10.1016/j.cell.2021.03.013
Singh J, Samal J, Kumar V, Sharma J, et al. Structure-Function Analyses of New SARS-CoV-2 Variants B.1.1.7, B.1.351 and B.1.1.28.1: Clinical, Diagnostic, Therapeutic and Public Health Implications. Viruses. 2021 Mar 9;13(3):439. doi: 10.3390/v13030439
Coutinho RM, Marquitti FMD, Ferreira LS, et al. Model-based estimation of transmissibility and reinfection of SARS-CoV-2 P.1 variant. medRxiv. Posted March 09, 2021. doi: 10.1101/2021.03.03.21252706
Faria NR, Mellan TA, Whittaker C, et al. Genomics and epidemiology of a novel SARS-CoV-2 lineage in Manaus, Brazil. medRxiv. Posted March 03, 2021. Publié le 14 avril 2021 dans Science. doi: 10.1126/science.abh2644
Voloch CM, Francisco Jr R da S, Almeida LGP de, et al. Genomic characterization of a novel SARS-CoV-2 lineage from Rio de Janeiro, Brazil. Journal of Virology. Posted Online 1 March 2021. doi: 10.1128/JVI.00119-21
Voloch CM, da Silva Francisco R, Jr., de Almeida LGP, et al. Genomic characterization of a novel SARS-CoV-2 lineage from Rio de Janeiro, Brazil. J Virol. 2021 Mar 1. doi: 10.1128/JVI.00119-21
Faria NR, Claro IM, Cândido D, et al. Genomics and epidemiology of a novel SARS-CoV-2 lineage in Manaus, Brazil. medRxiv. Posted March 03, 2021. doi: 10.1101/2021.02.26.21252554v1
Naveca F, Nascimento V, Souza V, et al. COVID-19 epidemic in the Brazilian state of Amazonas was driven by long-term persistence of endemic SARS-CoV-2 lineages and the recent emergence of the new Variant of Concern P.1. Research Square; 2021 Feb. doi: 10.21203/rs.3.rs-275494/v1
Sur le web :
P.1 (PANGO linages, grinch global report investigating novel coronavirus haplotypes)
Coronavirus : circulation des variants du SARS-CoV-2 (Santé publique France, 12 avril 2021)
COVID-19 : point épidémiologique en Guyane du 8 avril 2021 (Santé publique France,)
LIRE aussi : Covid-19 : le défi des nouveaux variants
Manaus, Brésil : de nouveaux variants du SARS-CoV-2 se jouent-ils de l’immunité collective ?
Grand merci pour toutes ces informations, pas simples à suivre pour un néophyte, mais je crois qu’on fait tous des progrès en biologie ces derniers temps (certains y croient même un peu trop…). Conclusion, si j’ai bien compris : on n’est pas près de laisser tomber les masques.
Bonjour et merci pour vos articles toujours intéressants.
Je ne l’ai peut-être pas vu passer dans l’article, mais qu’en est-il de l’efficacité du Coronavac par-rapport aux P1 et P2 ? Au Brésil on vaccine surtout avec Coronavac et Astra Zeneca, un peu de Pfizer aussi. Ici à Rio ce sont seulement les deux premiers qui sont disponibles selon les arrivages et les centres de vaccination, surtout Coronavac, et on a beaucoup de P1 (appelé variant amazonien ou variant de Manaus) et de P2 (appelé variant de Rio).
Concernant Le vaccin chinois Coronavac (développé par la société biopharmaceutique Sinovac) :
« Administration of at least one dose of CoronaVac showed effectiveness against symptomatic SARS-CoV-2 infection in the setting of epidemic P.1 transmission ». Effectiveness of CoronaVac in the setting of high SARS-CoV-2 P.1 variant transmission in Brazil: A test-negative case-control study (a retrospective, test negative, matched case-control study to estimate the effectiveness of CoronaVac).
Efficacy and safety of a COVID-19 inactivated vaccine in healthcare professionals in Brazil: The PROFISCOV study https://papers.ssrn.com/sol3/papers.cfm?abstract_id=3822780 (a randomised, double-blind, placebo-controlled phase 3 clinical trial with CoronaVac among healthy healthcare professionals in 16 centres in Brazil).
Cette étude, évaluant le vaccin Coronavac au Brésil, a été réalisée entre le 21 juillet et le 16 décembre 2020, donc avant l’émergence du variant P.1.
Merci pour cet article de grande qualité
La leçon à retenir est qu’il est très peu probable que la pandémie s’arrête d’elle même. Il y a en fait une course de vitesse entre le virus et ses mutations et la vaccination.
Il est donc crucial que la vaccination soit la plus rapide possible et ceux qui la ralentissent au prétexte d’effets secondaires rarissimes portent une lourde responsabilité.
Il sera aussi indispensable que les nouveaux vaccins répondant aux nouveaux variants soient mis en oeuvre sans être retardés par des essais à rallonge.
Enfin, « Force est de constater que la France ne brille pas par … », une fois de plus, hélas …
Bonjour, merci pour cet article et ce blog.
Merci pour cette brillante synthèse.